5 способов покраски металла и защиты его от ржавчины
Методы борьбы с коррозией железа, а попросту — ржавчиной имеют историю не менее долгую, чем история самого железа.
Еще викинги, отплывая в набег, обильно смазывали жиром стальные мечи и кольчуги для защиты от морской воды. Без этого ржавчина изгрызла бы металл еще до первого боя.
В наше время наиболее распространенным способом защиты от коррозии является окраска металла специальными составами.
Кто хоть раз держал в руках малярную кисть, подтвердит, что покраска не требует большого труда. Окрасить, скажем, ворота обычного гаража можно за час-полтора. Возможно немного больше, если учесть время на подготовку и на мытье инструмента по завершению работ.
Но представьте, что вам нужно окрасить не пять-семь квадратных метров, а тысячи и десятки тысяч, получая при этом гладкое, прочное покрытие? Тут уже кисточкой не обойтись, требуются совершенно иные решения и инструменты.

Давайте совершим экскурсию по цехам, где занимаются окраской, и посмотрим — как современные инженеры справляются с этой непростой задачей.
Краскопульт и окраска лакокрасочными составами
Начнем с популярного способа покраски — напыления с помощью краскораспылителя или иначе — краскопульта.
Существует три вида окраски краскопультом:
1. Безвоздушный.
Давление краски при этом процессе в сто раз сильнее, чем давление воды в кране домашнего водопровода. Вырываясь из сопла краскопульта, краска мгновенно распыляется, образуя конус или «факел» который направляют на деталь. Лишь немного затормозившись воздухом частицы краски буквально «вбиваются» в окрашиваемую поверхность.

2. Воздушный.
Краска вводится в струю воздуха, образуя воздушную смесь за счет вихревых процессов (турбулентности). Этот коктейль направляется на деталь, покрывая ее гладким, красивым и равномерным защитным слоем.
Давление при этом гораздо меньше, но наряду с рабочим факелом краски из ее мельчайших капель образуется туман. Это повышает расход состава и требует гораздо более дорогостоящих мер по защите работников и окружающей среды, чем при способе безвоздушном.
3. Комбинированный способ.
Краска выбрасывается под давлением порядка 20-30 атмосфер, а в ее факел дополнительно вводится сжатый воздух. Благодаря этому покрытие получается более равномерным, причем вредный туман не образуется.
Порошковая окраска
Альтернативой лакокрасочным составам стала изобретенная в 1950 году покраска порошковой краской.

Внешне процесс ее нанесения похож на напыление сжатым воздухом. Однако сразу бросается в глаза отсутствие «тумана» — взвеси краски в воздухе. Деталь словно сама притягивает краску, которая оседает на ней ровным слоем.
Притягивание обеспечивает электричество. Саму деталь заряжают положительным, а краску отрицательным зарядом высокого напряжения. И поскольку разноименные заряды притягиваются, краска прилипает к металлу, так же как прилипают кусочки бумаги к расческе потертой о волосы.
Затем деталь нагревают до температуры 200-250 градусов. Краска плавится и, растекаясь, образует тончайший, всего несколько десятков микрон, но прочный плотный слой.
Жесткие технологические требования, дорогое оборудование диктуют в полтора – два раза большую по сравнению с обычной краской стоимость. Тем не менее, высокое качество монолитных полимерных покрытий, позволяет им на равных конкурировать с традиционными, но и даже вытеснять их в ряде случаев.
На сегодня нанесение порошковых покрытий стало обычным делом, его можно заказать даже через Интернет http://oooprofpokraska.ru/metall/.
Окраска погружением в красящий состав
Даже электростатическое напыление все равно не гарантирует попадания краски в каждый уголок крупной, сложной детали. Например, кузова автомобиля.

Такие детали защищают от коррозии, погружая (окуная) деталь в ванну с краской. Этот способ позволяет окрасить даже внутренние полости, имеющие лишь несколько отверстий.
«А как выглядит окунаний?» — спросила меня однажды одна заказчица. Признаться, я ничего не понял, пришлось уточнить, что она имеет в виду. Оказалось, что она прочла на банке краски: «…наносить кистью, валиком, краскопультом либо окунанием» и логично предположила, что «окунаний» — это какой-то особый инструмент для окраски.
Защита металла металлом
Железную деталь можно окрасить не только краской или полимером, но и слоем другого металла. В отличие от железа многие металлы, например цинк, олово практически не поддаются коррозии.
Блестящее полированное покрытие образует тончайший слой хрома или никеля. Таким покрытием щеголяют самые разные детали, от никелированных смесителей для воды до хромированных деталей мотоциклов и автомобилей.

Не менее распространено лужение — покрытие тонким слоем олова. Из стальной жести покрытой изнутри и снаружи оловом делают всем известные консервные банки. Такая обработка сохраняет не только металл банки, но и ее содержимое.
Для нанесения защитного металла наиболее распространен электролитический способ. Деталь погружают в ванну с электролитом, и под воздействием электрического тока молекулы покрытия «налипают» на поверхность железа. Несмотря на то, что этот слой тоньше человеческого волоса служит он десятки лет.
Оксидирование или металл цвета воронова крыла
Если спросить у любого мужчины как называется темное покрытие пистолета или автомата, он тут же ответит — «воронение». Действительно черный или отливающий синеватым цвет оружия напоминает цвет перьев вороны, откуда и получил свое название.

Такое покрытие еще называют оксидирование или чернение. Как ни удивительно, черный защитный слой это окислы, химически аналогичные ржавчине. Защитные свойства обеспечивает им высокая плотность и упорядоченная структура.
Воронение довольно популярный способ защиты. Помимо оружия подвергают и самые разные детали и инструменты. В частности, популярные самонарезающие шурупы-«саморезы» так же получили черный цвет благодаря оксидированию.
Болезнь и лекарство
Произнося словосочетания «стальной характер», «железное слово» как синоним прочности и надежности мы не задумываемся — насколько беззащитным может быть железо.

Дырявые трубы отопления и кузова автомобилей, рухнувшие конструкции мостов и перекрытий — следствие неправильно сделанной или поврежденной окраски. Но лекарство от зубов ржавчины есть всегда, главное не затягивать с лечением, а еще лучше со своевременной профилактикой.
chonemuzhik.ru
способы защитить металл от ржавчины в быту, выбор покрытия
Интенсивное развитие производства стали, как правило, предполагает поиск новых средств и способов, которые позволяли бы предотвращать разрушение изделий из металла. Создание инновационных методик, связанных с защитой от коррозии, — это постоянный процесс. Изделия, сделанные практически из любого металла, могут терять свою работоспособность из-за воздействия химических и физических факторов извне. Последствия этого можно увидеть в виде ржавчины.

Разновидности коррозии
Перед тем как защитить металл от ржавчины, следует узнать о существующих видах. Способ обеспечения антикоррозийной защиты находится в прямой зависимости от условий применения деталей. Потому принято выделять следующие типы:- коррозия, которая связана с явлениями атмосферного характера;
- разрушение структуры металла в воде из-за наличия в ней солей и бактерий;
- деструктивные процессы, происходящие в грунте (почвенная коррозия).
Способы антикоррозионной защиты при этом должны подбираться в индивидуальном порядке, руководствуясь тем, в каких условиях будет эксплуатироваться изделие из металла.
Что касается типов поражения конструкций, то они могут быть следующими:
- ржавчина находится на всей поверхности изделия отдельными участками или сплошным покрытием;
- имеет вид пятен и проникает вглубь элемента;
- разрушает молекулы металла, приводя к трещинам;
- масштабное ржавление, при котором разрушается не только поверхность, но и более глубокие слои.
 Типы разрушения бывают и комбинированными. В некоторых ситуациях их очень сложно определить на глаз, особенно при точечном ржавлении.
Типы разрушения бывают и комбинированными. В некоторых ситуациях их очень сложно определить на глаз, особенно при точечном ржавлении.
Принято выделять химическую коррозию. При контакте с нефтяными продуктами, спиртами и иными агрессивными веществам происходит особая реакция, которая сопровождается высокой температурой и выделениями газа.
При электрохимической коррозии поверхность металлического сплава соприкасается с водой (электролитом). При этом осуществляется диффузия материала. Электролит обуславливает появление электротока, а электроны металла замещаются и приходят в движение, в результате чего возникает ржавчина.
Обеспечение защиты от коррозии и выплавка стальных изделий — две взаимосвязанные вещи. Коррозия причиняет существенный ущерб постройкам хозяйственного или промышленного назначения. Кроме того, этот процесс может привести к катастрофе, если говорить, например, об опорах электропередач, мостах, заграждениях и т. д.
Защита от коррозии в промышленности и быту
Необходимо обеспечить металлу надежную защиту от коррозии. Все условия, когда требуется защита металлов от коррозии, кратко можно поделить на промышленные и бытовые.
В промышленности существует несколько вариантов антикоррозийной защиты:
 Пассивация. В процессе производства в сталь добавляются другие металлические сплавы (молибден, никель, ниобий). Эти материалы характеризуются отличными эксплуатационными свойствами и высокой стойкостью к агрессивным воздействиям. Эти разновидности стали принято называть легированными.
Пассивация. В процессе производства в сталь добавляются другие металлические сплавы (молибден, никель, ниобий). Эти материалы характеризуются отличными эксплуатационными свойствами и высокой стойкостью к агрессивным воздействиям. Эти разновидности стали принято называть легированными.- Нанесение на поверхность стали каких-то других металлов. При этом на изделии образуется защитное покрытие. Зачастую для данной цели применяется алюминий, кобальт и хром.
- Применение специальных протекторов и анодов. При контакте детали с водой происходит разрушение протектора, который образует защитное покрытие. Такая методика часто используется в производстве деталей для морских буровых установок и судов.
Промышленные способы обеспечения антикоррозийной защиты очень разнообразны. К ним относится и покрытие специальной стекловолоконной эмалью, и химическая защита, и многие другие.
Антикоррозийная защита материала в домашних условиях подразумевает применение ЛКМ-покрытий и химических средств. Свойства защитного плана обеспечивают сочетанием разных элементов: смол на основе силикона, ингибиторов, полимеров, металлической стружки и пудры.
Следует отметить, что перед окрашиванием детали, ее нужно обработать специальным преобразователем коррозии или грунтовкой, иначе ее эксплуатационные свойства будут быстро уменьшаться.
Сегодня в продаже встречается несколько разновидностей преобразователей ржавчины:
- Средства-грунтовки. Характеризуются высокой адгезией с металлическими поверхностями, способствуют выравниванию покрытия перед покраской. Во многих грунтовках содержатся ингибиторы, тормозящие коррозийные процессы. Кроме того, заблаговременное нанесение слоя грунтовки позволяет сэкономить на окрашивании.
- Химические препараты. Преобразуют окись железа в более безопасные вещества, которым не страшна коррозия. Такие средства называются стабилизаторами.
- Составы, преобразующие ржавчину в обычные соли.
- Масла и смолы, уплотняющие и связывающие ржавчину, обеспечивая ее нейтрализацию.
Специалисты советуют подбирать краску и грунтовку какого-то одного производителя, чтобы их химический состав не имел особых отличий.
Краски для покрытия металлических изделий
Краски, предназначенные для обработки металлических поверхностей, бывают обычными и термостойкими. В большинстве случаев применяются три типа составов: эпоксидные, акриловые и алкидные. Есть и специальные краски антикоррозийного типа, которые обладают следующими достоинствами:
- эффективно защищают покрытие от атмосферных воздействий и перепадов температур;
- с легкостью наносятся валиком, кисточкой или распылителем;
- многие из них являются быстросохнущими;
- обладают широким выбором расцветок;
- отличаются долговечностью.
Что касается самых недорогих и доступных средств, то тут следует обратить внимание на обыкновенную серебрянку. В составе этого покрытия есть алюминиевая пудра, образующая защитную пленку на обработанном им изделии.
Этапы работ по борьбе с коррозией в быту
Методы борьбы с коррозией металлов предполагают определенную последовательность. Следует перечислить основные этапы этой работы:
 Перед тем как наносить преобразователь или грунтовую смесь, поверхность необходимо полностью очистить от маслянистых пятен, следов коррозии и различного рода загрязнений. Для этих мер можно воспользоваться болгаркой или щетками с металлическим ворсом.
Перед тем как наносить преобразователь или грунтовую смесь, поверхность необходимо полностью очистить от маслянистых пятен, следов коррозии и различного рода загрязнений. Для этих мер можно воспользоваться болгаркой или щетками с металлическим ворсом.- После этого можно приступать к нанесению слоя грунтовки, которая затем должна впитаться и как следует просохнуть.
- Далее на поверхность наносится пара слоев. Перед тем как наносить второй слой, нужно дождаться полного высыхания первого. В процессе работы обязательно нужно пользоваться защитными очками, перчатками и специальным респиратором, так как все применяемые вещества и составы являются токсичными.
Антикоррозийная защита металлических сплавов — очень непростой процесс. В промышленности он начинается на стадии расплавления стали. Производители ЛКМ-покрытий занимаются совершенствованием своей продукции, увеличивая ее долговечность и стойкость.
obrabotkametalla.info
Защита от коррозии и окрашивание металла
В бытовых условиях чаще приходится иметь дело со сталью, цинком и алюминием.
Сталь в свою очередь можно подразделить на две категории:
- легированная или «нержавейка»;
- не легированная (углеродная).
Виды металлов и их характеристики
В составе легированной стали помимо железа находятся примеси других металлов, в основном хрома. У такой стали на поверхностях образуются оксиды, защищающие весь сплав от коррозии.
Углеродная сталь лишена подобной защиты. В ней железо имеет прямой контакт с кислородом, водой, солями, и вступая с ними в реакцию? постепенно превращается в оксид железа, или проще говоря, – в ржавчину.
Углеродную сталь может защитить цинковое покрытие. Сталь с такой защитой называется оцинкованной. Цинк намного лучше противостоит агрессивным средам. Даже в местах механических повреждений этого покрытия, цинковые соединения образуют защитную пленку на поверхности железа.
Алюминий практически не реагирует на атмосферные воздействия. Потому, что оксид алюминия, всегда присутствующий на поверхности этого металла, весьма прочен, и в химическую реакцию в обычных условиях не вступает.
Исключение могут составить лишь случаи, когда алюминий соседствует с солями меди, или подвергается точечному воздействие концентрированных составов щелочи и кислот.
Таким образом, алюминий, оцинковку, легированную сталь чаще красят в целях декорации, или для создания дополнительной долговременной защиты от коррозии.
Основные же проблемы возникают с обычной углеродной сталью, которая, кстати, наиболее часто используется, вследствие своей дешевизны.
Для защиты углеродной стали от атмосферных воздействий необходимо провести ее специальное окрашивание, т.е. создать на поверхности искусственный защитный и декоративный слой.
Виды защит от коррозии
Все защиты металлов от ржавчины можно условно разделить на две категории:
- пассивные, которые просто препятствуют доступу кислорода и воды к поверхности металла;
- активные, которые имеют в своем составе ингибиторы, взаимодействующие со ржавчиной и таким образом блокирующие ее развитие.
Создавая защиту металла от коррозии, рекомендуется всегда совмещать эти два вида, — пассивную и активную защиты.
Пассивная защита
- Нитроэмали.
Часто применявшиеся в прошлом для окрашивания металла, сейчас проигрывают другим составам по многим параметрам, в том числе и по устойчивости к воде и по устойчивости к жирам.Они менее эластичны, и разрушаются при вибрациях которые присутствуют в конструкциях, но могут быть и не заметными для человека.
- Алкидные краски.
Применяются наиболее часто, вследствие высоких потребительских качеств, включая и цену. Они имеют отличные изолирующие и эстетические свойства. - Битумные составы.
Они неплохо себя зарекомендовали, к тому же их намного проще использовать, чем краски – достаточно нанести один неказистый слой. Но применяться они могут скорее в скрытых местах, так как их декоративные свойства не на высоте. - Кремнийорганические эмали.
Имеют повышенную устойчивость к воздействию высоких температур, и к перепадам температуры. Им свойственны отличные красящие свойства. Они предают поверхности хороший цвет и блеск. - Водоэмульсионные краски.
Создают не столь эффективную антикоррозийную защиту. Требуют значительно более устойчивой «подложки» на поверхности металла. - Преобразователи ржавчины.
Составы, вступающие в реакцию с окислами железа, образуют дополнительную защитную пленку. Чаще делаются на основе ортофосфорной кислоты.Активная защита
Для активной защиты применяются специальные вещества – ингибиторы ржавчины. Ими в первую очередь дополняются грунтовки для металла. Но и преобразователи ржавчины и даже сами декоративные краски могут содержать подобные ингредиенты, что придает им новые антикоррозийные свойства.
Сами по себе простые краски, даже очень качественные, не создают достаточно долговечный, прочный и надежно связанный с металлом слой. На сегодняшний день срок службы пассивного защитного слоя, нанесенного по чистому металлу, может составить максимум 3 – 4 года.
С активной защитой срок службы покрытия сразу увеличивается до 10 – 15 лет.
Общий порядок работ по окрашиванию
- Удаление ржавчины механическим путем и с помощью химического преобразователя.
- Нанесение антикоррозийного ингибиторного состава.
- Нанесение пассивной защиты
Процессы, выполняемые при стандартном окрашивании
:
- Старая краска и ржавчина удаляются стальной щеткой вручную.
- При необходимости, для удаления применяется механизация – дрель или шлифовальная машинка (болгарка) оснащенные стальной щеткой.
- Поверхность дополнительно матируется наждачной бумагой. Это увеличивает площадь соприкосновения и сцепляемость грунта с металлом.
- Поверхность тщательно очищается ветошью от пыли и частиц ржавчины. Для этих целей применяется также кисть и пылесос.
- Поверхность обрабатывается преобразователем ржавчины.
- Металл покрывается специальной грунтовкой содержащей элементы активной защиты в точном соответствии с заводской инструкцией.
- Наносится первый слой краски.
- Наносятся вторичные слои краски. Для нанесения краски может применяться кисть, валик, или распылитель. Краска наносится точно в соответствии с заводской инструкцией.
Рекомендации
При выполнении работ обращайте внимание на охрану труда. Составы могут быть пожароопасными и токсичными. Электроинструмент – травмоопасным.
Чтобы результат был качественным, соблюдайте инструкцию по применению материала. Поверхность должна быть обезжиренной и сухой. Температура окружающего воздуха и его влажность – в соответствии с инструкцией по применению материалов.
Также не лишним будет придерживаться нижеследующих рекомендаций.Соседние поверхности конструкций, которые не подлежать окрашиванию, накрываются полиэтиленовой пленкой и скотчем.
Применение термофена для удаления старой краски не эффективно, ввиду высокой теплопроводности металла. Очистку необходимо вести механическим путем.
Отдельные преобразователи ржавчины могут содержать в себе ингибиторы, и создавать весьма прочную пленку на поверхности металла. С такими преобразователями применение грунтовки становится не обязательным.
Всегда предпочтительнее несколько слоев краски вместо одного.
Лучше использовать составы одного производителя. Они «увязаны» между собой.
Упрощенная покраска
Во многих случаях, когда металлические детали не подвержены сильному воздействию вредной среды (перепады температуры, вода, лед, соли, ультрафиолетовое излучение) и находятся внутри помещений, процесс покраски можно упростить.
Можно применить специальные антикоррозийные краски, содержащие в своем составе и преобразователь ржавчины, и ингибиторы и собственно лако-красочную пассивную защиту, т.е. три в одном. Срок службы таких покрытий – порядка 7 лет.
Как и при обычном окрашивании, необходимо сперва очистить поверхность, и чем качественнее это будет сделано – тем лучше. Затем нужно нанести грунтовочный слой той же самой краской «три в одном».Но для этого ее необходимо разбавить на 10 – 25 % растворителем. После высыхания грунтовочного слоя наносятся 2 или 3 слоя уже густой краски.
Что продается?
Например, в продаже можно встретить следующие составы и краски для защиты и окрашивания металла.
- Преобразователи ржавчины:
- «Зебра» (Украина) – около 100 грн за 0,5 л.
- Kompozit (Украина) – 25 грн за 1 л.
- Glutoglean (Германия) – порядка 130 грн за 0,75 л.
- Грунтовки по металлу:
- «Прогресс-2010» (Украина) – 50 грн за 1 кг.
- Alpina metallgrund (Германия) -100 грн за 0,75 кг.
- Rostex super (Финляндия) – 150 грн за 1 кг.
- Korrostop (Эстония) – 100 грн за 1 кг.
- Краски.
- «Ржавостоп» — 60 грн за 0,9 л.
- Alpina metallgrund (Германия) — 100 грн за 0,75 л.
- Hammerite (Англия) – 130 грн за 0,75 л.
- Panser (Финлядния) – 130 грн. за 0,9 л.
Для правильного подбора составов конечно же лучше будет проконсультироваться со специалистом. Для этого ему надо дать информацию об окрашиваемых поверхностях, условиях их эксплуатации и необходимом сроке службы. Наиболее дорогие составы выбирать не всегда разумно, тем более не стоит слишком экономить и приобретать «неизвестного производителя». Консультация практикующего специалиста в этих вопросах часто необходима.Если вы все же хотите сделать окрашивание не самостоятельно, а привлечь наемных мастеров, то следует быть готовым к тому, что стоимость самих материалов от общих затрат составят примерно одну треть. А две трети потребуется отдать за работу по очистке металла и за нанесение всех слоев защиты и краски.
stroy-block.com.ua
Коррозия металлов и способы защиты от неё
Коррозия – разрушение поверхности сталей и сплавов под воздействием различных физико-химических факторов – наносит огромный ущерб деталям и металлоконструкциям. Ежегодно этот невидимый враг «съедает» около 13 млн. т металла. Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери. А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Что такое коррозия и её разновидности
Основной причиной интенсивного окисления поверхности металлов (что и является основной причиной коррозии) являются:
- Повышенная влажность окружающей среды.
- Наличие блуждающих токов.
- Неблагоприятный состав атмосферы.
Соответственно этому различают химическую, трибохимическую и электрохимическую природу коррозии. Именно они в совокупности своего влияния и разрушают основную массу металла.
Химическая коррозия
Такой вид коррозии обусловлен активным окислением поверхности металла во влажной среде. Безусловным лидером тут является сталь (исключая нержавеющую). Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4. Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.

Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях. Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Электрохимическая коррозия
Эта разновидность коррозии более коварна: разрушение металла в данном случае происходит при совокупном влиянии воды и почвы на стальную поверхность (например, подземных трубопроводов). Влажный грунт, являясь слабощёлочной средой, способствует образованию и перемещению в почве блуждающих электрических токов. Они являются следствием ионизации частиц металла в кислородсодержащей среде, и инициирует перенос катионов металла с поверхности вовне. Борьба с такой коррозией усложняется труднодоступностью диагностирования состояния грунта в месте прокладки стальной коммуникации.
Электрохимическая коррозия возникает при окислении контактных устройств линий электропередач при увеличении зазоров между элементами электрической цепи. Помимо их разрушения, в данном случае резко увеличивается энергопотребление устройств.
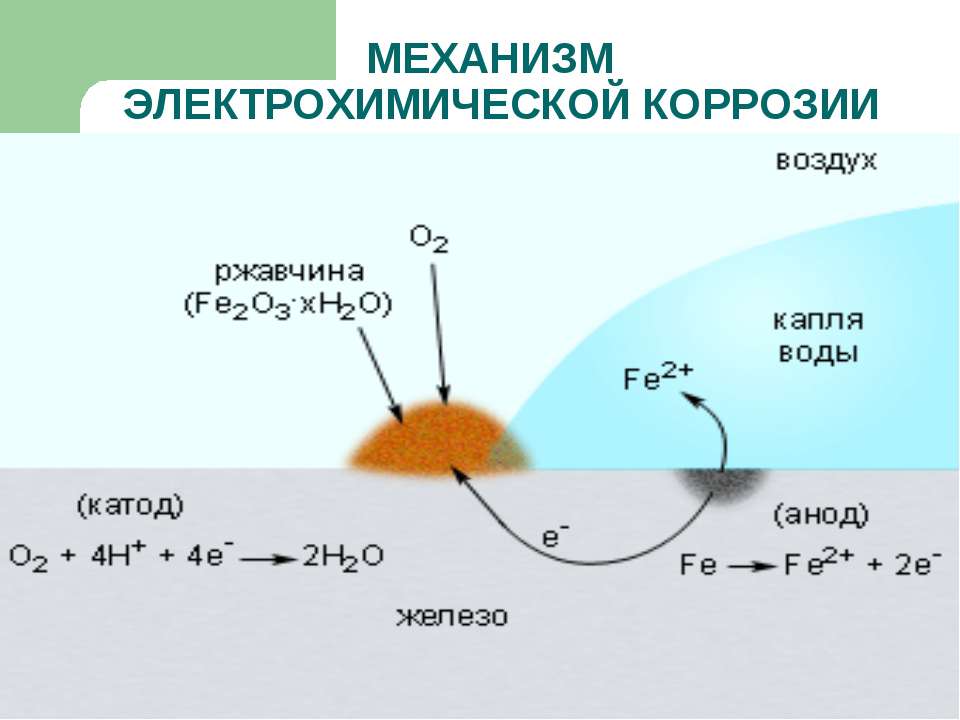
Трибохимическая коррозия
Данному виду подвержены металлообрабатывающие инструменты, которые работают в режимах повышенных температур и давлений. Антикоррозионное покрытие резцов, пуансонов, фильер и пр. невозможно, поскольку от детали требуется высокая поверхностная твёрдость. Между тем, при скоростном резании, холодном прессовании и других энергоёмких процессах обработки металлов начинают происходить механохимические реакции, интенсивность которых возрастает с увеличением температуры на контактной поверхности «инструмент-заготовка». Образующаяся при этом окись железа Fe2O3 отличается повышенной твёрдостью, и поэтому начинает интенсивно разрушать поверхность инструмента.

Методы борьбы с коррозией
Выбор подходящего способа защиты поверхности от образования ржавчины определяется условиями, в которых работает данная деталь или конструкция. Наиболее эффективны следующие методы:
- Нанесение поверхностных атмосферостойких покрытий;
- Поверхностная металлизация;
- Легирование металла элементами, обладающими большей стойкостью к участию в окислительно-восстановительных реакциях;
- Изменение химического состава окружающей среды.
Механические поверхностные покрытия
Поверхностная защита металла может быть выполнена его окрашиванием либо нанесением поверхностных плёнок, по своему составу нейтральных к воздействию кислорода. В быту, а также при обработке сравнительно больших площадей (главным образом, подземных трубопроводов) применяется окраска. Среди наиболее стойких красок – эмали и краски, содержащие алюминий. В первом случае эффект достигается перекрытием доступа кислороду к стальной поверхности, а во втором – нанесением алюминия на поверхность, который, являясь химически инертным металлом, предохраняет сталь от коррозионного разрушения.
Положительными особенностями данного способа защиты являются лёгкость его реализации и сравнительно небольшие финансовые затраты, поскольку процесс достаточно просто механизируется. Вместе с тем долговечность такого способа защиты невелика, поскольку, не обладая большой степенью сродства с основным металлом, такие покрытия через некоторое время начинают механически разрушаться.

Химические поверхностные покрытия
Коррозионная защита в данном случае происходит вследствие образования на поверхности обрабатываемого металла химической плёнки, состоящей из компонентов, стойких к воздействию кислорода, давлений, температур и влажности. Например, углеродистые стали обрабатывают фосфатированием. Процесс может выполняться как в холодном, так и в горячем состоянии, и заключается в формировании на поверхности металла слоя из фосфатных солей марганца и цинка. Аналогом фосфатированию выступает оксалатирование – процесс обработки металла солями щавелевой кислоты. Применением именно таких технологий повышают стойкость металлов от трибохимической коррозии.
Недостатком данных методов является трудоёмкость и сложность их применения, требующая наличия специального оборудования. Кроме того, конечная поверхность изменяет свой цвет, что не всегда приемлемо по эстетическим соображениям.
Легирование и металлизация
В отличие от предыдущих способов, здесь конечным результатом является образование слоя металла, химически инертного к воздействию кислорода. К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина. Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения. При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.

Изменение состава окружающей среды
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция. Это может быть вакуумирование (для сравнительно небольших объектов), или работа в среде инертных газов (аргон, неон, ксенон). Данный метод весьма эффективен, однако требует дополнительного оборудования — защитных камер, костюмов для обслуживающего персонала и т.д. Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Кто нам мешает, тот нам поможет
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них — закиси-окиси Fe3O4. Данное вещество образуется при температурах 250…5000С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку. Присутствуя на поверхности заготовки, Fe3O4 перекрывает доступ кислороду воздуха при полугорячей деформации металлов и сплавов, и тем самым блокирует процесс зарождения трибохимической коррозии. Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов. Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически.
blastingservice.ru
это? Виды и способы защиты от коррозии на металлических изделиях
Коррозия металла – это ржавчина, в первую очередь, которая образовалась на поверхности, чем больше ржавчины, тем глубже она проникает и разрушает материал элемента.
Любую коррозию возможно охарактеризовать тремя признаками:
- Во-первых, это восстановительно-окислительный процесс.
- Во-вторых, этот процесс является самопроизвольным, то есть возникает в любых условиях.
- В-третьих, процесс коррозии чаще всего возникает и распространяется на поверхности элемента, и иногда проникает вглубь.

Коррозия металла — это процесс, который проходит в химических или электрохимических средах, он приводит к повреждению верхних слоев материала.
Коррозии поддаются не только металлические изделия, но и бетонные, а также керамические.
Виды коррозии по характеру разрушения
На материале может протекать коррозия двух видов:
- Сплошная – распространена на всей поверхности изделия. Такой вид также делится на несколько подвидов:
- Равномерная – ржавчина появляется в одинаковом количестве на всех участках изделия.
- Неравномерная – ржавчина появляется с разной скоростью на разных участках.
- Избирательная – разрушению подвергается определенный компонент металлического сплава.
- Местная – коррозия образуется на отдельных небольших по размеру участках на поверхности детали. Выражается в единичных углублениях, раковинах и коррозирующих точках.

Виды коррозии металлов по механизму протекания
Существует несколько причины возникновения коррозии металла, химия этих процессов на сегодняшний день достаточно изучена, что помогает эффективно бороться с разрушением материалов.
Химическая коррозия металлов – происходит между металлом и средой, протекает окислительно-восстановительная реакция. Данный вид коррозии характерен для такой среды, в который не может протекать электрический ток. Химическая коррозия по условию протекания может быть:
- При газовой коррозии ржавчина возникает в результате воздействия на металл газовой среды чаще всего при высоких температурах. Особенностью этого вида является то, что воздействие газовой среды на некоторые металлы приводит к их полному разрушению, но на некоторых металлах (цирконий, алюминий, хром) протекающая реакция оставляет лишь защитную пленку.
- Жидкостная поверхностная коррозия возникает при воздействии жидких агрессивных сред, также без возможности протекания электрического тока.
Электрохимическая коррозия – эта реакция имеет место быть только в средах, где возможно протекание электрического тока.
Электрохимическая коррозия имеет возможность протекать в самых разных средах, но все они делятся на два типа по условию протекания:
- Коррозия с участим электролитов в растворах– протекает в среде кислот, соли, воде, оснований.
- Коррозия в атмосферных условиях – является самой часто встречающейся коррозией.
Виды коррозии по условиям протекания
Как было отмечено выше, по условиям протекания коррозия может быть газовой, жидкостной, атмосферной или в растворах электролитов. Необходимо сделать этот список более полным, поэтому ниже раскрыты дополнительные типы коррозии:
- Коррозия металлов, протекающая в почвах и грунтах;
- Биокоррозия, возникающая вследствие жизнедеятельности микроорганизмов на поверхности материала;
- Структурная — возникает из-за неоднородной структуры металла;
- Контактная коррозия проявляется при долгом соприкосновении металлов с различными потенциалами в электролите;
- Трение материала в коррозийной среде;
- Коррозия, возникающая от трения материала в коррозийной среде;
- Фреттинг-коррозия проявляется во время возникновения колебаний в коррозийной среде;
- Кавитация появляется при воздействии существующей коррозийной среды и ударного воздействия извне.

Результат коррозии
Пластинчатая коррозия металла – вид на протекающий процесс
Основные типы атмосферной коррозии
Принято выделять три основных типа атмосферной коррозии: влажная, мокрая, сухая. Жидкая и мокрая, в силу способности проводить электрический ток, протекают по электрохимическим законам, а сухая по химическим.
- Влажная глубокая коррозия металла будет протекать там, где на металле можно наблюдать тонкую влажную пленку. В зависимости от происходящего в окружающей среде, на пленке может образовываться конденсат, после чего начинается процесс коррозийного разрушения.
- Мокрая коррозия начинается на поверхности хорошо увлажненной, при относительной влажности окружающей среды около 100%. Капли, образовавшиеся на поверхности, помогают коррозийному износу.
- Сухая атмосферная коррозия менее агрессивна, потому что процесс разрушения протекает при малой влажности воздуха. Образовавшаяся на изделии пленка замедляет образование ржавчины.

Закорродировавший корабль
Виды коррозии бетона
Бетон является крепким каменным строительным материалом, состоящим из цемента, наполнителя и связующих веществ. Так как этот материал эксплуатируется в условиях открытой окружающей среды, а также нередко в агрессивно-опасных средах, то он так же подвержен коррозийному износу.

Схема коррозии на бетоне
Существует несколько видов бетонной коррозии:
- В результате взаимодействия с окружающей средой, на поверхности бетона могут образовываться легкорастворимые соли, которые при взаимодействии с внутренними компонентами материала приводят к его разрушению.
- Часто встречающаяся проблема – это разъединение составных частей цементного камня водой или вымывание гидроксида кальция, который образовывается в процессе такой реакции или ранее.
- В условиях окружающей среды, в состав бетона проникают вещества, которые имеют достаточно большой объем, в сравнении с исходными продуктами реакции, что приводит к механическим и химическим повреждениям целостности материала, далее эти участки под воздействием окружающей среды начинают коррозировать про принципу 1 или 2.
При коррозии бетона, невозможно выявить только одну причину, зачастую образовавшаяся коррозия – продукты нескольких факторов в совокупности.
Коррозия железа и меди
Коррозия железа
Давно выявлено, что зачастую коррозия (ржавчина) на железных элементах возникает вследствие протекания реакций окисления воздухом или кислотами – окислительно-восстановительные реакции. Как и в любом металле, ржавчина захватывает верхние слои железного изделия и возникает химическая коррозия, электрохимическая или электрическая.
Если рассмотреть каждый этот процесс в отдельности то получится, что при химическом возникновении ржавчины происходит переход электронов на окислитель, в результате образовывается оксидная пленка, а реакция выглядит так:
3Fe + 2O2 = Fe3O4 (FeO•Fe2O3)
Образовавшаяся пленка не защищает материал от дальнейшего возникновения окислительно-восстановительных реакций, она свободно пропускает воздух, что способствует образованию новой ржавчины.
При электрохимической коррозии, которая чаще всего возникает с железом в грунте, протекает реакция с образованием свободного кислорода и воды, если они остаются на железном элементе, то это вызывает новые продукты коррозии.
Fe + O2 + h3O → Fe2O3 · xh3O
Электрическая коррозия железа является самой непредсказуемой, так как возникает из-за блуждающих токов, которые могут попадать к железному элементу от линий электропередач, трамвайных путей, крупногабаритного электрооборудования и другое. Блуждающий ток запускает процесс электролиза металла, а он способствует образованию ржавых пятен.
Коррозия меди
При эксплуатации медных элементов необходимо учитывать причины коррозии, зачастую они обусловлены средой, где находится элемент. Например, в таких средах как: атмосферная, морская вода, при контакте с галогеновыми веществами и в слабых растворах солей медь коррозирует стабильно медленно.
1)Cu+2h3SO4→CuSO4+SO2↑+2h3O
2)Cu+h3SO4→CuO+SO2↑+h3O
Также медь подвергается коррозии в обычных атмосферных условиях:
2Cu+h3O+CO2+O2→ CuCO3*Cu(OH)2

Методы и способы защиты металлов от коррозии
Вследствие того, что коррозийный процесс протекает на верхних слоях металла конструкции, то защита поверхности заключается в создании верхнего защитного слоя для изделия, который убирает следы коррозии на металле. Такими защитными покрытиями выступают вещества металлические и неметаллические.
Важно понимать, что защита от коррозии не избавляет от нее, а лишь замедляет уже происходящие процессы. Однако, если верно подобрать средство борьбы, то возможно замедлить процесс образования коррозии на несколько лет.
Исходя из названия, металлические покрытия – это вещества, в основе которых металл. Например, чтобы защитить конструкцию из железа от коррозии на ее поверхность наносят слои цинка, меди или никеля.

Очистка труб от коррозии
Неметаллические покрытия – специальные вещества, наиболее широкая группа защитных соединений. Они изготавливаются в виде красок, эмалей, смазок, грунтовок, составов на битумной и битумно-полимерной основе и т.д.
Большая популярность неметаллических соединений в устранении следов коррозии заключается в их широком выборе, большом ценовом диапазоне, легкости изготовления и хороших защитных свойствах.
Наименьшую популярность приобрели химические покрытия из-за необходимости проводить сложные химические процессы:
- Оксидирование – образование оксидных пленок на поверхностях защищаемых деталей.
- Азотирование – насыщение верхних слоев материала азотом.
- Цементация – реакция, при которой верхние слои соединяются с углеродом и т.д.
Также при коррозии металлов существуют способы защиты, при которых на этапе сплавления металлов в них вводят специальные соединения, которые смогут повысить коррозийную устойчивость будущего материала.
Большую группу защиты представляют способы электрохимической и протекторной защиты.
Электрохимическая защита состоит в процессе преобразования продуктов коррозии в среде электролитов с помощью проводящего электрического тока. Постоянный ток присоединяется к катоду (защищаемому материалу), а в качестве анода выступает проводящий металлический источник, который при своем разрушении защищает объект от ржавчины.

Электрохимическая защита от коррозии
Протекторная защита протекает по такому же принципу, однако вместе металлического связующего изделия выступают специальные изделия – протекторы, которые выступают в роли анода. В результате протекающей реакции, протектор разрушается, защищая катод (конструкцию из металла).
Таким образом, хоть коррозия является необратимым процессом, но на данный момент люди научились эффективно замедлять ее губительное воздействие.
corprotect.ru
Коррозия. Виды и способы защиты от коррозии
Коррозия материалов является одной из важных мировых проблем. Практика показывает, что только прямые безвозвратные потери металла от коррозии составляют 10…12% всей производимой стали, при этом суммарный ущерб в промышленных странах достигает 4-5% от национального дохода. Ведь корродирует не только черный металл ( сталь, чугун, железо и некоторые его сплавы ), но и бетон, дерево, камень, даже полимеры. Наиболее интенсивная коррозия наблюдается в зданиях и сооружениях химических производств, что объясняется действием различных газов, жидкостей и мелкодисперсных частиц непосредственно на строительные конструкции, оборудование и сооружения, а также проникновением этих агентов в грунты и действием их на фундаменты. Агрессивному воздействию подвержено до 75% строительного фонда. Коррозия металла приводит к ослаблению конструктива и, как следствие, снижению безопасности эксплуатации сооружений.

Коррозия – процесс разрушения материалов вследствие химических или электрохимических процессов. По характеру самого процесса коррозию разделяют на две основные группы : химическую и электрохимическую. Химическая коррозия протекает в не электролитах – жидкостях, не проводящих электрического тока и в сухих газах при высокой температуре. Электрохимическая коррозия происходит в электролитах и во влажных газах и характеризуется наличием двух параллельно идущих процессов: окислительного (растворение металлов) и восстановительного (выделение металла из раствора).
По внешнему виду коррозию различают: пятнами, язвами, точками, внутрикристаллитную, подповерхностную. По характеру коррозионной среды различают следующие основные виды коррозии: газовую, атмосферную, жидкостную и почвенную.
Газовая коррозия происходит при отсутствии конденсации влаги на поверхности. На практике такой вид коррозии встречается при эксплуатации металлов при повышенных температурах.
Атмосферная коррозия относится к наиболее распространенному виду электрохимической коррозии, так как большинство металлических конструкций эксплуатируются в атмосферных условиях. Коррозия, протекающая в условиях любого влажного газа, также может быть отнесена к атмосферной коррозии.
Жидкостная коррозия в зависимости от жидкой среды бывает кислотная, щелочная, солевая, морская и речная. По условиям воздействия жидкости на поверхность металла эти виды коррозии получают добавочные характеристики : с полным и переменным погружением, капельная, струйная. Кроме того, по характеру разрушения различают коррозию равномерную и неравномерную.
По степени воздействия на металлы коррозионные среды делятся на неагрессивные, слабоагрессивные, среднеагрессивные и сильноагрессивные.
Бетон и железобетон находят широкое применение в качестве конструкционного материала при строительстве зданий и сооружений химических производств. Но они не обладают достаточной химической стойкостью против действия кислых сред. Свойства бетона и его стойкость в первую очередь зависит от химического состава цемента из которого он изготовлен. Наибольшее применение в конструкциях и оборудовании находят бетоны на портландцементе. Причиной пониженной химической стойкости бетона к действию минеральных и органических кислот является наличие свободной гидроокиси кальция (до 20%), трехкальциевого алюмината (3CaO×Al2O3) и других гидратированных соединений кальция.
Коррозия бетона происходит тем интенсивнее, чем выше концентрация водных растворов кислот. При повышенных температурах агрессивной среды коррозия бетонов ускоряется. Несколько более высокой кислотостойкостью обладает бетон, изготовленный на глиноземистом цементе, из-за пониженного содержания оксида кальция. Кислотостойкость бетонов на цементах с повышенным содержанием оксида кальция в некоторой степени зависит от плотности бетона. При большей плотности бетона кислоты оказывают на него несколько меньшее воздействие из-за трудности проникновения агрессивной среды внутрь материала.
Щелочестойкость бетонов определяется главным образом химическим составом вяжущих, на которых они изготовлены, а также щелочестойкостью мелких и крупных заполнителей.
Увеличение срока службы строительных конструкций и оборудования достигается путем правильного выбора материала с учетом его стойкости к агрессивным средам, действующим в производственных условиях. Кроме того, необходимо принимать меры профилактического характера. К таким мерам относятся герметизация производственной аппаратуры и трубопроводов, хорошая вентиляция помещения, улавливание газообразных и пылевидных продуктов, выделяющихся в процессе производства; правильная эксплуатация различных сливных устройств, исключающая возможность проникновения в почву агрессивных веществ; применение гидроизолирующих устройств и др.
Непосредственная защита металлов от коррозии осуществляется нанесением на их поверхность неметаллических и металлических покрытий либо изменением химического состава металлов в поверхностных слоях: оксидированием, азотированием, фосфатированием.
Для защиты поверхностей от коррозии существуют разнообразные покрытия: лакокрасочные (антистатичные и армированные, полиуретановые, акриловые, порошковые эпоксидно – полиэфирные, органосиликатные и кремнийорганические), металлизационные с цинком, алюминием, медью и комбинациями этих металлов. Это краски, лаки, эмали, тонкодисперсные порошки, пленки. Лакокрасочные покрытия вследствие экономичности, удобства и простоты нанесения, хорошей стойкости к действию промышленных агрессивных газов нашли широкое применение для защиты металлических и железобетонных конструкций от коррозии. Защитные свойства лакокрасочного покрытия в значительной степени обуславливаются механическими и химическими свойствами, сцеплением пленки с защищаемой поверхностью.
Лакокрасочные материалы в зависимости от назначения и условий эксплуатации делятся на десять групп:
- А – покрытия стойкие на открытом воздухе;
- АН – то же, под навесом;
- П – то же, в помещении;
- Х – химически стойкие;
- Т – термостойкие;
- М – маслостойкие;
- В – водостойкие;
- ХК – кислотостойкие;
- ХЩ – щелочестойкие;
- Б – бензостойкие.
Наиболее распространены в промышленности покрытия металлические, неметаллические (органического и неорганического происхождения), а также покрытия, образованные в результате химической и электрохимической обработки металла.
Выбор вида покрытия зависит от условий, в которых используется защищаемое изделие (перепад температур, повышенная влажность, морская или пресная вода, щелочь, кислота, соли металлов, радиация, электроток и огонь), и технологичность возможностей формирования покрытия.
Наиболее часто применяемые способы защиты металлов:
- легирование;
- электрохимическая защита;
- покрытие металлами;
- защитные пленки.
Легирование – это введение в металл на стадии его производства определенного количества специальных добавок, например – хрома или марганца. Это придает сталям особые свойства, необходимые для использования в сложных условиях. Для возведения современных зданий, особенно повышенной этажности, необходима высококачественная атмосферостойкая легированная сталь, например, погодоустойчивая марка COR-TEN. Такой материал позволяет решить проблемы эксплуатации сооружений даже в экстремальных климатических условиях.
Одними из самых популярных и относительно недорогих мер защиты от коррозии сегодня являются методы, изменяющие химический состав металла в поверхностных слоях. Как правило, это электрохимические способы нанесения покрытий на металл. Наиболее известный процесс называется оцинковкой, которая в зависимости от способа обработки металла делится на горячую и холодную. В первом случае обрабатываемый материал погружается в специальную ванну. Затем под воздействием переменного тока осуществляется его обработка в растворе фосфата цинка при плотности тока 4 А/дм², напряжении 20 В и температуре 600-700ºС. В результате электрохимической реакции образуется ферроцинковый сплав. При применении второго способа на подготовленную поверхность стального листа наносится защитный слой из цинка. Оцинковка толщиной 0,3 мм позволяет обеспечить защиту обработанной поверхности металла более чем на 30 лет.
Итальянская фирма «Metalnastri» разработала метод, сочетающий в себе качество горячего и технологичность холодного цинкования. Это простая идея наклейки цинковой фольги на стальную поверхность. Высокую антикоррозийность создает сплошной цинковый слой, а токопроводящие клеевые композиции обеспечивают и электрохимическую защиту поверхности.
ЦНИИПСК им. А.П. Мельникова предложил метод термодиффузионного цинкования (ТДЦ) метизных и малогабаритных изделий из стали и чугуна. Метод заключается в нагреве металлоизделий в среде, содержащей порошок цинка. В результате на поверхности изделия образуется цинковое покрытие с хорошими защитными и декоративными свойствами. Технологический процесс такого цинкования экологически чист и практически безотходен. В качестве сырья используются отечественные материалы, не требующие специальной обработки. ТДЦпокрытие обладает высокой адгезией и износостойкостью, обеспечиваемой в результате взаимной диффузии железа и цинка. Срок службы покрытия в 1,5-4 раза больше по сравнению с традиционными цинковыми покрытия.
Широкое распространение цинковых покрытий обусловлено их хорошими химическими свойствами. Для стали (катод) цинк является анодом, за счет этого образуется гальваническая пара, имеющая высокие защитные свойства, хорошо сохраняемые даже при малой толщине слоя. Скорость разрушения цинкового покрытия составляет примерно 1-10 мкм в год в зависимости от различных факторов. Оцинковка может осуществляться совместно с другими металлами – с добавлением алюминия (Al) или железа (Fe). В настоящее время в России широко используется сталь Galfan c цинкоалюминиевым покрытием и сталь Galvannealed с цинкожелезным покрытием.
При покрытии другими металлами в зависимости от вида коррозии покрывающий слой наносят различными способами. В качестве покрывающего материала часто используется хром или никель. Хромирование – электролитическое нанесение покрытия из хрома на поверхность металлического изделия. Никелирование, также нанесение на поверхность изделий никеля толщиной от 2 до 50 мкм.
На практике обычно применяются следующие методы:
- Погружение изделий в расплавленный металл (горячий способ). Заключается в том, что изделия погружают в ванну с расплавленным металлом или же нагретую поверхность деталей обволакивают расплавленным металлом.
- Метод термической диффузии. Основан на диффузии (проникновении) в поверхностные слои деталей присадок при высокой температуре. Диффузионные покрытия наносятся при нагреве деталей в твердой (порошкообразной), жидкой или газообразной фазе металла.
- Металлизация. Заключается в нанесении (распылении) на поверхность деталей слоя присадок расплавленного металла с помощью пульверизаторов.
- Контактный метод осаждения металла. Осуществляется без применения внешнего источника тока за счет вытеснения менее благородными металлами более благородных из растворов их солей. Толщина таких покрытий невелика и защитные свойства их невысоки.
Следует отметить, что металлические покрытия достаточно хорошо защищают металл от коррозии. Однако при нарушении защитного слоя она может протекать даже более интенсивно, чем без покрытия. Поэтому в промышленности для улучшения свойств металлических поверхностей, обработанных электротехническим методом, используется способ нанесения защитных покрытий из полимерных материалов. Такие продукты получили широкое распространение в строительной индустрии. Использование полимерных материалов для антикоррозионной защиты обусловлено их уникальными физико-химическими показателями. Полимеры имеют небольшой удельный вес, высокую стойкость к не механическим воздействиям (соприкосновение с водой, солями, щелочами или кислотами). Обладают пластичностью и светостойкостью. В настоящее время наибольшее распространение получили « трехслойные» продукты с двойным уровнем защиты. Первый уровень – непосредственно оцинковка, второй – полимер. Благодаря такой структуре сталь становится стойкой к воздействию агрессивных сред, механическим повреждениям и ультрафиолетовому изучению. Срок их службы составляет порядка 50 лет, в зависимости от качества и толщины покрытия. Необходимо также учесть, что высокие эксплуатационные характеристики таких материалов напрямую зависят от качества оцинковки исходного металла, а потребительские качества – от применяемого в составе полимера.
Альтернативой полимерным материалам являются конструкционные пластмассы и стеклопластики, получаемые на основе различных синтетических смол и стекловолокнистых наполнителей. В настоящее время выпускается значительный ассортимент материалов, особое место среди них занимает полиэтилен. Он инертен во многих кислотах, щелочах и растворителях, а также имеет высокую теплостойкость.
Другим направлением использования полиэтилена в качестве химически стойкого материала является порошковое напыление. Применение полиэтиленовых покрытий объясняется их дешевизной и хорошими защитными свойствами. Покрытия легко наносятся на поверхность различными способами, в том числе пневматическим и электростатическим распылением.
Защитные пленки. Способ заключается в нанесении на металл защитной оболочки из различных компонентов в следующей последовательности: шпатлевка, грунтовка, краска, лак или эмаль.
Для противокоррозионной защиты конструкций зданий и сооружений (ферм, ригелей, балок, колонн, стеновых панелей), а также наружных и внутренних поверхностей емкостного технологического оборудования, трубопроводов, газоводов, воздуховодов вентиляционных систем, которые в процессе эксплуатации не подвергаются механическим воздействиям абразивных частиц, применяют лакокрасочные покрытия. Такие покрытия наиболее эффективны для защиты от атмосферной коррозии. Однако срок службы лакокрасочных покрытий невелик и составляет 4-5 лет. Для повышения коррозионной стойкости лакокрасочных покрытий используют различные противокоррозионные пигменты.
Следует назвать антикоррозионные пигменты фирмы SNCZ (Франция): фосфаты цинка; модифицированные фосфаты цинка; фосфаты, не содержащие цинк; полифосфаты; феррит кальция, а также тетраоксихромат цинка; хроматы стронция, цинка, бария.
Наиболее часто используются фосфаты цинка PZ 20 и PZ W2 в большинстве лакокрасочных систем: органоразбавляемых, водоразбавляемых, воздушной и горячей сушки.
Там, где нельзя использовать противокоррозионные пигменты, содержащие цинк (контакт с пищевыми продуктами), используются пигменты на основе щелочеземельных фосфатов Новинокс РАТ 30, Новинокс РАТ 15 и Новинокс РС01.
Металлоконструкции, подвергающиеся воздействию соляного тумана, могут быть защищены лакокрасочными материалами, содержащими фосфат щелочеземельных металлов. Фосфат щелочеземельных металлов – нетоксичный пигмент, что повышает экологичность лакокрасочного покрытия и увеличивает сферу его применения.
Тетраоксихромат цинка ТС 20, хромат стронция L203E и хромат цинка CZ20 – применяются в лакокрасочных материалах, использующихся в авиационных, судовых покрытиях, а также в составе адгезивов для легких сплавов.
Для защитных покрытий, эксплуатирующихся в условиях высоких температур (до 600ºС), используются хромат бария М 20 и феррит кальция FC 71. Применение феррита кальция для защитных покрытий – новое направление в лакокрасочных материалах. В табл. 1 представлена стойкость различных лакокрасочных материалов (ЛКМ) к агрессивным средам.
Таблица 1. Стойкость лакокрасочных материалов
| ЛКМ, по типу связующего | Стойкость к агрессивным средам | |||||||
| Вода | Водяной пар | Растворители | Разбавленные растворители | Кислоты | Разбавленные кислоты | Щелочи | Разбавленные щелочи | |
| Винилхлоридные | + | ++ | ± | ± | ± | + | ± | + |
| Хлоркаучуковые | + | ++ | ± | ± | ± | + | ± | + |
| Акриловые | ± | ++ | ± | ± | ± | + | ± | + |
| Алкидные | ± | + | ± | + | ± | ± | ± | ± |
| Битумные | ++ | ++ | ± | ± | ± | ± | ± | + |
| ПУ ароматические | ± | ++ | + | ++ | + | + | ± | ± |
| ПУ алифатические | + | ++ | ± | + | ± | + | ± | ++ |
| Эпоксиднополиуретановые | ++ | ++ | ± | ± | ± | + | + | ++ |
| Эпоксидные | ++ | ++ | + | ++ | ± | + | ++ | ++ |
| Цинк-силикатные | + | ++ | ++ | ++ | + | + | + | + |
| Перхлорвиниловые | ++ | ++ | ± | ± | ± | ± | ± | + |
Примечания: ++ отлично, + хорошо, ± удовлетворитльно
Наиболее распространенным способом защиты от коррозии строительных конструкций, сооружений и оборудования является использование неметаллических химически стойких материалов: кислотоупорной керамики, жидких резиновых смесей, листовых и пленочных полимерных материалов (винипласта, поливинилхлорида, полиэтилена, резины), лакокрасочных материалов, синтетических смол и др. Для правильного использования неметаллических химически стойких материалов необходимо знать не только их химическую стойкость, но и физико-химические свойства, обеспечивающие условия совместной работы покрытия и защищаемой поверхности. При использовании комбинированных защитных покрытий, состоящих из органического подслоя и футеровочного покрытия, важным является обеспечение на подслое температуры, не превышающей максимальной для данного вида подслоя.
Для листовых и пленочных полимерных материалов необходимо знать величину их адгезии с защищаемой поверхностью. Ряд неметаллических химически стойких материалов, широко используемых в противокоррозионной технике, содержит в своем составе агрессивные соединения, которые при непосредственном контакте с поверхностью металла или бетона могут вызвать образование побочных продуктов коррозии, что, в свою очередь, снизит величину их адгезии с защищаемой поверхностью. Эти особенности необходимо учитывать при использовании того или иного материала для создания надежного противокоррозионного покрытия.
Просмотров: 1 089
extxe.com
Как защитить металл от коррозии, варианты средств
Такая проблема как ржавчина, знакома всем. Ржавеют не только металл, но и сплавы, содержащие в своем составе металл. Данная проблема не может быть полностью истреблена, так как сам окружающий климат при взаимодействии с металлами оказывает негативное влияние. Для борьбы с коррозией современный рынок предлагает обширный выбор средств. Начиная список от красок, и заканчивая различными растворами и очистителями.
Коррозия не просто уничтожает огромное количество металла, последствия коррозии уходят далеко вглубь и вредят экономики мира. Если не бороться данной проблемой, то последствия будут губительнее с каждым годом.

Последствия коррозии металлов:
- коррозия приводит к понижению уровня эффективности работы металлоконструкций;
- огромные финансовые потери в результате разрушения трубопроводов, деталей машин, судов, мостов, паровозов и т.п;
- простоит производства из-за выхода из строя оборудования и испорченных металлических деталей, приводит к простоям сырья и готовой продукции;
- загрязнение продукции, как следствие снижение её качества.
Использование специальных антикоррозийных защитных покрытий. Для того чтобы средство эффективно справлялось с проблемой оно должно обладать рядом свойств:
- износостойкость и твердость;
- высокий уровень адгезии;
- близкая по значению величина теплового расширения с величиной металлоконструкции;
- максимальное ограждение от негативных воздействий окружающей среды.
Использование органических неметаллических покрытий. Одним из самых доступных и практичных средств является лакокрасочное покрытие.

Во-первых, такой способ отличается:
- экономичностью;
- использованием различных расцветок, что придает некоторую эстетичность внешнему виду металлоконструкции;
- элементарностью восстановления защитного слоя, в ситуации его повреждения.
Данный способ имеет и ряд негативных свойств:
- низкий уровень термостойкости;
- низкий уровень влагостойкости;
- низкий уровень устойчивости к механическим воздействиям.

Использование неметаллических неорганических покрытий. Один из более эффективных средств является создание защитной пленки на металлической конструкции при химическом воздействии. Чаще всего покрывают металл фосфатной или оксидной пленкой.
- фосфатные пленки. Используются в качестве защиты цветных и черных металлов. Изделие опускается в раствор цинка или марганца с кислыми солями. В ходе реакции на металле образуется защитная пленка и уже на нее можно наносить краску или лак. Такой способ более эффективный, чем просто покрытие пленкой или лаком;
- оксидные пленки. Наносится в случае, когда геометрические данные нужно оставить в неизменном виде, например, точные приборы, оружие.
Использование электрохимического способа защиты от коррозии
Такой способ защиты подходит в случае, если металл подвергся поляризации.
Электрохимическая защита бывает:
- Катодная. Используется для сплавов, в состав которых входит железо, для нержавеющей и углеродистой стали. Способ защиты довольно прост: коррозийное изделие, подключается к катодному протектору или к «+» источника тока. (Подходят все элементы с высоким положительным потенциалом, углерод, свинец, тантал и другие)
- Анодная. Данный способ используется для очистки, (внутренней части аппаратов, подземных сооружений, конструкции, касающиеся или находящиеся в соленой воде). Способ защиты довольно прост: коррозийное изделие, подключается к электродному потенциалу « — « источника тока.
Выбирать лучше всего комбинирующие средства защиты, например антикоррозийные краски уже содержащие фосфатную пленку. Отталкиваться стоит от степени ржавления и того, что это за металлоконструкция какого размера и предназначения.
fanera-info.ru
 Пассивация. В процессе производства в сталь добавляются другие металлические сплавы (молибден, никель, ниобий). Эти материалы характеризуются отличными эксплуатационными свойствами и высокой стойкостью к агрессивным воздействиям. Эти разновидности стали принято называть легированными.
Пассивация. В процессе производства в сталь добавляются другие металлические сплавы (молибден, никель, ниобий). Эти материалы характеризуются отличными эксплуатационными свойствами и высокой стойкостью к агрессивным воздействиям. Эти разновидности стали принято называть легированными. Перед тем как наносить преобразователь или грунтовую смесь, поверхность необходимо полностью очистить от маслянистых пятен, следов коррозии и различного рода загрязнений. Для этих мер можно воспользоваться болгаркой или щетками с металлическим ворсом.
Перед тем как наносить преобразователь или грунтовую смесь, поверхность необходимо полностью очистить от маслянистых пятен, следов коррозии и различного рода загрязнений. Для этих мер можно воспользоваться болгаркой или щетками с металлическим ворсом.